炔烃是药物分子、天然产物和有机材料中普遍存在的多功能性官能团,随着Au(I)、Pt(II)和其他亲电金属催化剂的发展,炔烃化学也得到了十足的发展。因此,如何在有机分子中选择性引入炔烃引起了化学家们的广泛关注。但是,经典的交叉偶联方法必须要对起始原料进行预官能团化(如引入卤化物、不饱和键等)。近年来,已出现了所谓的inverse-Sonogashira反应,即利用过渡金属催化剂直接对活化和未活化的C(sp2)-H键进行炔基化反应。然而,颇具挑战的C(sp3)-H键的直接炔基化反应仍难以实现。通常情况下,C(sp3)-H键炔基化反应可通过自由基途径进行(图1a),只需要通过1,5-HAT活化或者α-位含有杂原子的C-H键活化就可实现良好的区域选择性。此外,也可以通过C-H键活化途径实现C(sp3)-H键炔基化反应,但是需要有导向基团(如β-螯合羧酸衍生物或杂环化合物,图1b)。
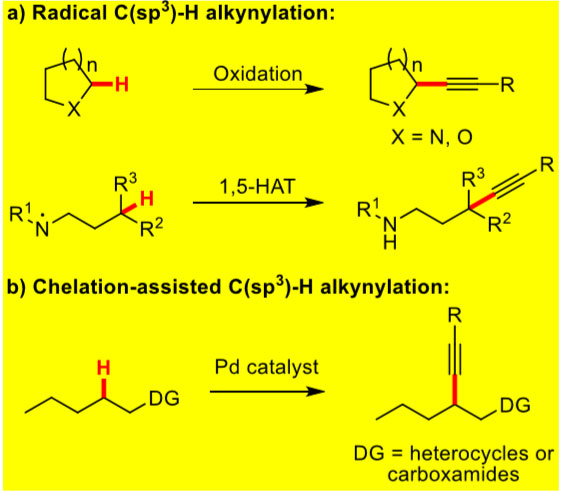
图1. 金属催化C(sp3)-H的炔基化。图片来源:Angew. Chem. Int. Ed.
酮肟作为导向基团已被广泛应用于过渡金属催化的C(sp3)-H键官能团化中,例如C-H键氧化(J. Am. Chem. Soc., 2004, 126, 9542–9543; Org. Lett., 2005, 7, 4149–4152)、酰胺化(Chem. Commun., 2018, 54, 11096–11099; Chem. Commun., 2014, 50, 12073–12075; J. Am. Chem. Soc., 2014, 136, 4141–4144)、胺化(Org. Lett., 2018, 20, 6260–6264)、芳基化(J. Am. Chem. Soc., 2015, 137, 12231–12240; Chem. Sci., 2016, 7, 1383–1387)和碘化反应(J. Am. Chem. Soc., 2017, 139, 12394–12397)。受此启发,西班牙加泰罗尼亚化学研究所(ICIQ)的Antonio M. Echavarren课题组设想:能否实现衍生自醛、酮或醇的肟的炔基化反应,从而拓宽C(sp3)-H键的官能团化范围?近日,他们实现了铱催化的脂肪族肟的β-炔基化反应(图2),该反应的特点在于它仅对一级C(sp3)-H键具有选择性,并可用于复杂分子的后期修饰。相关成果发表在Angew. Chem. Int. Ed. 上。
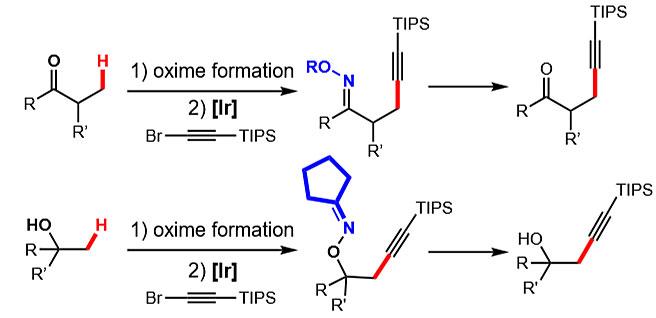
图2. Ir-催化的肟C(sp3)-H键炔基化。图片来源:Angew. Chem. Int. Ed.
在先前的研究中,作者发现Cp*Rh(III)催化剂和溴代炔烃是一种高活性体系(ACS Catal., 2018, 8, 2166–2172),可广泛应用于芳香族和烯烃C(sp2)-H键的炔基化反应中。然而,将该体系扩展到脂肪族肟1a的C(sp3)-H键上时,并未成功。随后,作者对反应条件进行优化,最终发现使用Cp*Ir(III)催化剂、TIPS保护的溴代炔烃2a、AgSbF6、Ag2CO3、添加剂LiOAc以及溶剂1,2-二氯乙烷(DCE),并在70℃下反应14 h,能以78%的产率获得甲基炔基化产物3a。对照实验表明反应中任一组分都是必不可少的。使用其他金属催化剂、其他银盐、其他溶剂或者降低催化剂的负载量、升高或降低温度都会降低3a的产率,甚至反应无法进行。用溴代或碘代炔烃2b-2d均未观察到转化(图3)。
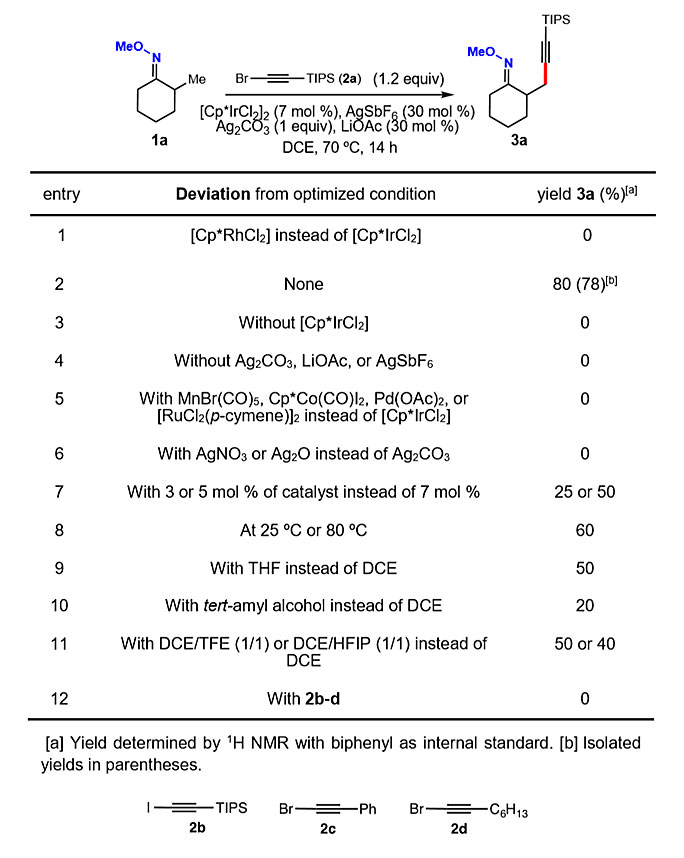
图3. 反应条件优化。图片来源:Angew. Chem. Int. Ed.
在最优条件下,作者对底物范围进行了考察(图4)。肟醚1a-1c以相似的产率(70-78%)得到3a-3c(图4),且未观察到底物1b上的肟甲基发生炔基化反应。然而,2-甲基环己酮的游离肟、丙酮肟和O-烯丙基肟都未能得到β-炔基化产物。2-甲基-2-环己烯酮(1d)、2,5-二甲基苯醌(1e)和(+)- trans-二氢香芹酮(1f)的甲基肟都能以中等的收率得到炔基化产物3d-3f。值得一提的是,(R)-香芹酮甲基肟(1g)的炔基化反应能以克级规模制备,并以良好的产率获得3g。有趣的是,(L)-葑酮衍生物1h选择性地在桥头甲基上发生炔基化反应,以72%的收率得到3h。非环状酮和醛的甲基肟1i-1m也能以中等至较好的产率得到相应的炔基化产物3i-3m。
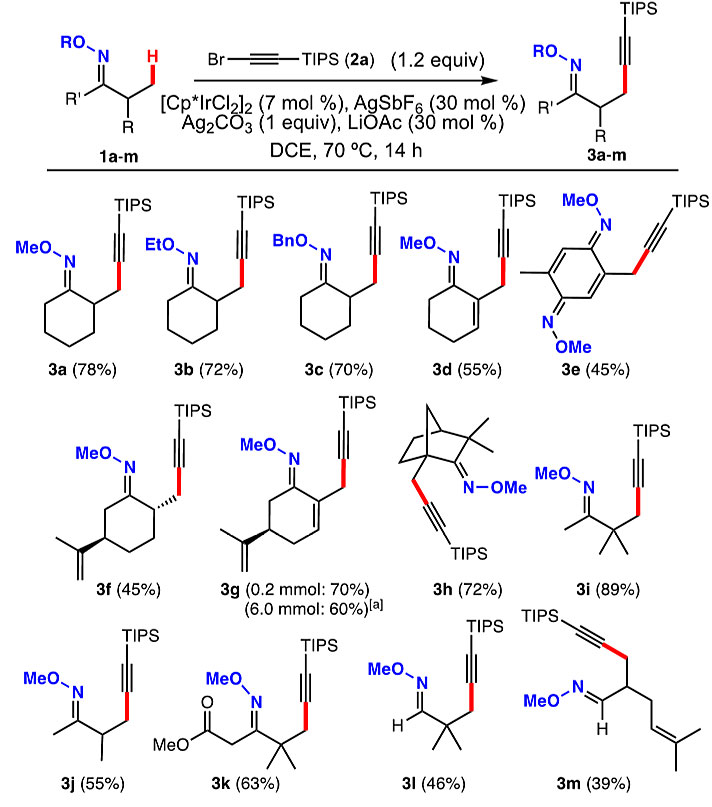
图4. 底物扩展一。图片来源:Angew. Chem. Int. Ed.
随后,作者将炔基化反应的底物范围扩展到醇类衍生的肟(图5)。首先,以1-甲基环己醇为底物,考察了不同的肟类化合物,结果显示环戊酮肟4a的收率最高,以89%的收率得到炔基化衍生物5a。伯醇(5d)、仲醇(5e-m)和叔醇(5n-o)都能兼容该反应,以44-80%的收率得到炔基化产物,并且可以耐受醚(5i)、芳环(5j)以及大位阻的金刚烷基(5m)。所有的反应均显示出对C-H键活化的选择性,也就是说,反应是通过五元环铱中间体进行的,产物5f的形成也证实了这一过程,因为反应在醇的α-位甲基进行炔基化反应,而不是β-位甲基。有趣的是,即使底物(5k)的β-位存在C(sp2)-H键,仍在α-位甲基上进行炔基化反应。

图5. 底物扩展二。图片来源:Angew. Chem. Int. Ed.
然而,当底物的β-位带有羧基、酯、酮、酰胺、胺或O-硫代氨基甲酸酯等官能团时,反应无法进行。但是,含氮杂环化合物(如吡啶6a-6c、吡唑6d、吡嗪6e)在120 °C时就能以较好的收率得到C-H键炔基化产物7a-7e(图6)。
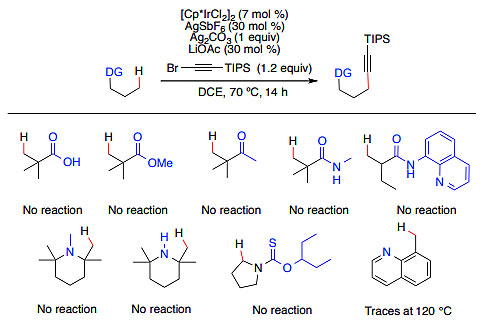

图6. Ir-催化氮杂环导向的C(sp3)–H键炔基化。图片来源:Angew. Chem. Int. Ed.
此外,该反应还可用于天然产物的酮肟衍生物的后期官能团化(图7)。例如(-)-山道年的酮肟衍生物(8a)能以77%的收率得到炔基化产物3n;齐墩果酸(8b)通过一系列标准转化和炔基化反应后,分别以35%和20%的收率得到可分离的3o和3o′混合物;羊毛甾醇(8c)能以63%的收率和4∶1的非对映体混合物转化为3p。

图7. 山道年(8a)、齐墩果酸(8b)和羊毛甾醇(8c)通过甲氧肟衍生物的官能团化。图片来源:Angew. Chem. Int. Ed.
最后,作者对产物进行了衍生化。在TBAF的作用下,便可将3g和5a中的硅基脱保护,产率分别为85%和95%(图8a)。在酸性条件下用甲醛处理,可以使甲肟3a脱保护得到相应的酮9a(图8b),产率为81%。此外,也可用LiAlH4将肟5还原为醇10a,产率为89%。或者用NaCNBH3和过量的Zn粉,也可以76-79%的产率还原为醇10b-10d。有趣的是,该步骤也可分步进行,即在NaCNBH3的作用下,以83%的收率分离出羟胺11。然后在锌粉的存在下还原,得到10e,收率72%。
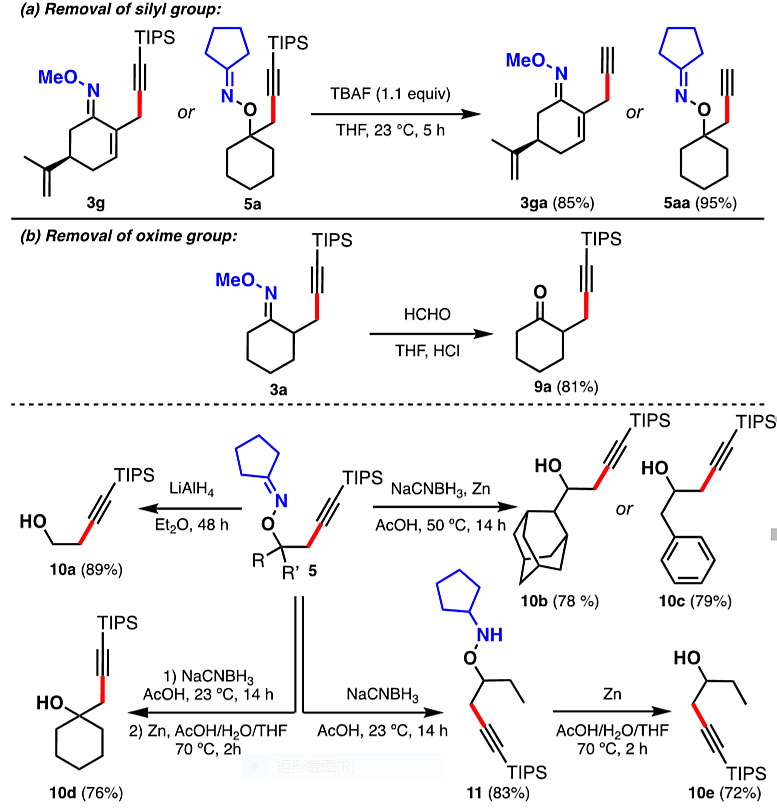
图8. 炔的脱保护及肟的脱除。图片来源:Angew. Chem. Int. Ed.
总结
Antonio M. Echavarren课题组开发了一种铱催化的脂肪族肟(源于醛、酮、醇衍生物)的β-炔基化反应。该反应对一级C(sp3)-H键具有选择性,并且可以耐受酯、醚、烯烃等官能团。环状和非环状脂肪族底物(包括天然产物的衍生物)也能兼容该反应。此外,碱性杂环如吡啶、吡唑或吡嗪也可以作为导向基团实现这一转化。该方法为天然产物及药物分子的后期修饰提供了一条简单、高效的方法。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Iridium-Catalyzed β-Alkynylation of Aliphatic Oximes as Masked Carbonyl Compounds and Alcohols
Eric Tan, Margherita Zanini, Antonio M. Echavarren
Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202002948
 实验外包
实验外包
 方案定制
方案定制
 仪器预约
仪器预约
 技术研发
技术研发
